礼来公司于当地时间4月17日公布了其在研口服小分子胰高血糖素样肽-1(GLP-1)受体激动剂Orforglipron的首个3期ACHIEVE-1临床试验积极关键结果,试验评估了与安慰剂相比,orforglipron在患有二型糖尿病且仅通过饮食和锻炼血糖控制不充分的成人中的安全性和有效性,数据显示,该药物在血糖控制、体重管理及安全性方面展现出与注射型GLP-1药物相当的疗效。
与需要注射的传统GLP-1受体激动剂(如Ozempic)不同,Orforglipron是一种在研、每日一次的小分子(非肽类)口服GLP-1受体激动剂,可在全天任何时间服用,无需饮食或饮水方面的限制。礼来公司目前正在开展Orforglipron的3期临床试验,用于治疗2型糖尿病以及用于肥胖或超重且至少存在一种体重相关疾病的成年人的体重管理。此外,该药物还被研究用于治疗肥胖成年人的阻塞性睡眠呼吸暂停和高血压。
礼来公司预计在今年年底向全球监管机构提交orforglipron用于体重管理,并预计在2026年提交用于治疗二型糖尿病的监管申请。
ACHIEVE-1(NCT05971940)是一项为期40周的3期随机双盲安慰剂对照试验,旨在比较单用orforglipron 3mg、12mg和36mg与安慰剂单独治疗患有二型糖尿病且仅通过饮食和运动血糖控制不充分的成人的疗效和安全性。该试验以1:1:1:1的比例将美国、中国、印度、日本和墨西哥的559名参与者随机分组,接受3mg、12mg或36mg的orforglipron或安慰剂。
本研究的目的是证明在第1次访视前至少90天内未服用任何抗糖尿病药物且未接受过胰岛素治疗的二型糖尿病患者中,与安慰剂相比,40周后orforglipron (3mg、12mg、36mg)在降低糖化血红蛋白(A1C)方面优于基线。研究参与者的糖化血红蛋白在≥7.0%和≤9.5%之间,身体质量指数≥23 kg/m2。orforglipron治疗组的所有参与者均以每日一次1mg的orforglipron剂量开始研究,然后以四周为间隔逐步增加剂量,直至最终随机维持剂量3mg(以1mg为增量)、12mg(以1mg、3mg和6mg为增量)或36mg(以1mg、3mg、6mg、12mg和24mg为增量)。不允许灵活用药。
分析显示,在第40周时,orforglipron达到主要终点,即相较安慰剂显著降低糖化血红蛋白(A1C)水平,平均从基线的8.0个百分点下降了1.3至1.6个百分点(采用疗效估计量分析)。在关键次要终点方面,超过65%的患者在使用最高剂量orforglipron后,其A1C降至≤6.5个百分点,低于美国糖尿病协会(ADA)定义的糖尿病诊断阈值。
此外,在另一关键次要终点中,接受最高剂量orforglipron治疗的患者平均体重减轻16.0磅(7.9%),且患者在研究结束时尚未达到体重减轻平台期。
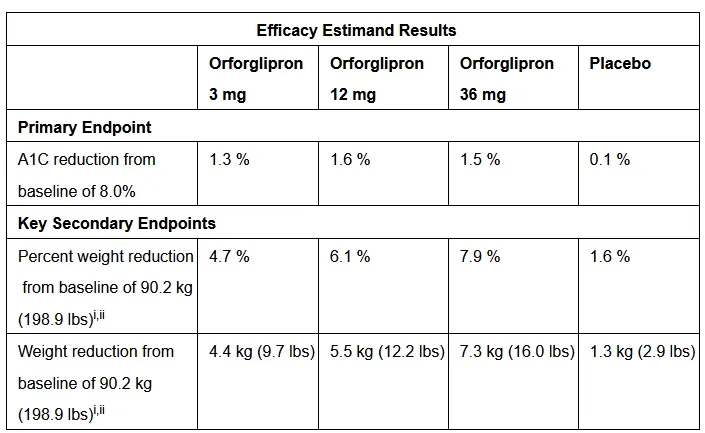 3期ACHIEVE-1临床试验结果
3期ACHIEVE-1临床试验结果
对于治疗方案的要求,每一剂量的orforglipron均导致统计学上显著的A1C降低。在体重的关键次要终点中,12mg和36mg剂量导致统计学上显著的减少。
• A1C降低幅度:1.2%(3mg)、1.5%(12mg)、1.5%(36mg)、0.4%(安慰剂)
• 体重减轻百分比:4.5%(3mg)、5.8%(12mg)、7.6%(36mg)、1.7%(安慰剂)
• 体重减轻数值:4.2公斤(9.3磅;3mg)、5.2公斤(11.5磅;12mg)、7.2公斤(15.8磅;36mg)、1.5公斤(3.4磅;安慰剂)
在ACHIEVE-1研究中,orforglipron的整体安全性特征与GLP-1类药物的既有安全性一致。最常见的不良事件与胃肠道相关,且大多为轻度至中度。Orforglipron组(3mg、12mg和36mg)的常见不良事件包括:腹泻(19%、21%、26%,VS 安慰剂9%)、恶心(13%、18%、16%,VS 安慰剂2%)、消化不良(10%、20%、15%,VS 安慰剂7%)、便秘(8%、17%、14%,VS 安慰剂4%)和呕吐(5%、7%、14%,VS 安慰剂1%)。因不良事件导致的治疗中断的比例分别为6%(3mg)、4%(12mg)、8%(36mg),对比安慰剂的1%。未观察到肝脏安全性信号。
参考来源:
Lilly's oral GLP-1, orforglipron, demonstrated statistically significant efficacy results and a safety profile consistent with injectable GLP-1 medicines in successful Phase 3 trial. Retrieved April 17, 2025.
注:以上资讯来源于网络,由香港济民药业整理编辑(如有错漏,请帮忙指正),只为提供全球最新上市药品的资讯,帮助中国患者了解国际新药动态,仅供医护人员内部讨论,不作任何用药依据,具体用药指引,请咨询主治医师。
如您发现本网站有文字编辑或内容错误,请点击此处发送(需要安装有foxmail或outlook支持),
或发邮件至:info@pidrug.com,香港济民药业感谢您的到访!
欢迎您添加香港济民药业微信,或在公众号内留言。




