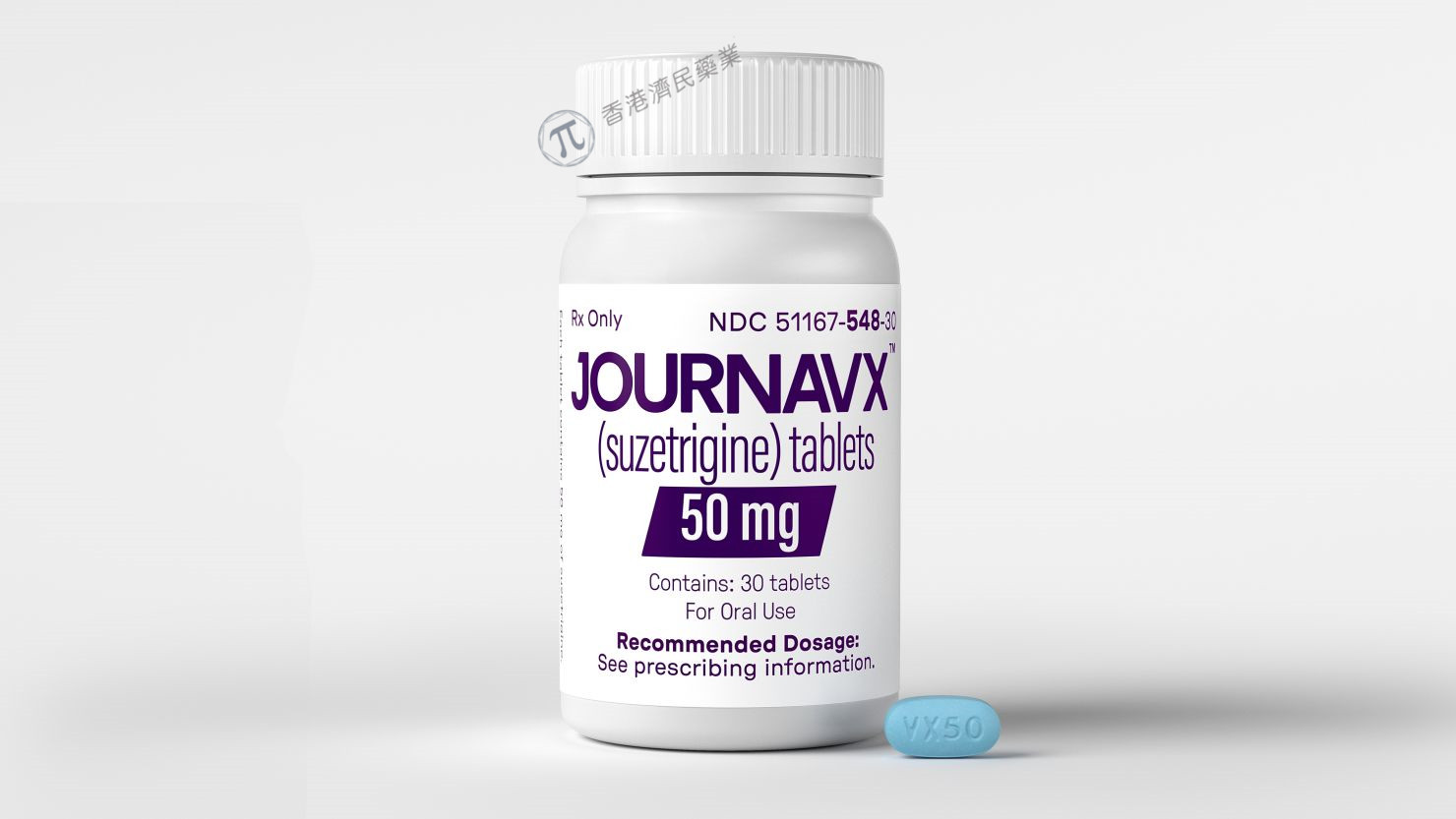
2025年1月30日,Vertex制药公司宣布美国食品药品监督管理局(FDA)批准Journavx(suzetrigine,曾用名VX-548)50毫克口服片剂,用于治疗成人中度至重度急性疼痛。Journavx此前曾获得美国FDA授予突破性疗法认定、快速通道资格和优先审评资格。
Journavx是一种口服选择性NaV1.8抑制剂,与其它NaV离子通道相比,它对NaV1.8具有高度选择性。NaV1.8是在外周神经系统的痛觉信号传导中起到关键性作用的电压门控钠通道。Vertex制药称,Journavx旨在通过选择性抑制NaV1.8,干预疼痛信号传导路径,在疼痛信号传递至大脑之前减轻疼痛。
这是FDA所批准的首款基于新机制的非阿片类止痛药物。与阿片类药物相比,该药物可能在提供更好镇痛效果的同时,避免上瘾等副作用。
该批准基于两项3期随机、双盲、安慰剂对照试验的数据,这些试验评估了suzetrigine在腹部成形术(ClinicalTrials.gov标识符:NCT05558410)和拇趾囊肿切除术(ClinicalTrials.gov标识符:NCT05553366)后的疗效和安全性。
为了符合这些试验的条件,参与者必须在腹部成形术完成后4小时内或在拇趾囊肿切除术后停止区域麻醉后9小时内,在口头分类评分系统中具有中度至重度疼痛,并且在数字疼痛评分量表(NPRS)中具有4分或更高的疼痛评分。
这两项研究的主要终点是suzetrigine组与安慰剂组以及氢可酮酒石酸氢盐/对乙酰氨基酚(HB/APAP)组相比,0至48小时疼痛强度差异的时间加权总和(SPID48)。
在腹部成形术试验中,患者被随机分配接受suzetrigine(n=447)、安慰剂(n=223)或HB/APAP (n=448)。研究结果显示,与安慰剂相比,suzetrigine在减轻疼痛方面具有统计学显著优势(SPID48的最小二乘[LS]平均差异,48.4 [95% CI,33.6–63.1];P <.0001)。据报道,suzetrigine组出现有意义疼痛缓解的中位时间(定义为NPRS≥2分)为119分钟,安慰剂组为480分钟。
在拇囊炎切除术研究中,患者被随机分配接受suzetrigine (n=426)、安慰剂(n=216)或HB/APAP (n=431)。结果显示:suzetrigine与安慰剂相比具有更好的疼痛缓解效果(SPID48的LS平均差异为29.3 [95% CI,14.0-44.6];P =.0002)。据报道,suzetrigine组疼痛缓解的中位时间为240分钟,安慰剂组为480分钟。
在两项试验中均未发现Suzetrigine在SPID48上优于HB/APAP(腹部成形术:SPID48的LS平均差异,6.6[95% CI ,-5.4,18.7];拇趾囊肿切除术:在SPID48,-20.2 [95% CI,-32.7,-7.7]中的LS平均差异。
suzetrigine最常见的不良反应包括瘙痒、肌肉痉挛、肌酸磷酸激酶升高和皮疹。服用强效CYP3A抑制剂的患者禁用本品,严重肝功能损害(Child-Pugh C级)的患者应避免使用本品。
Journavx以50毫克片剂的形式提供。起始剂量为口服100毫克,应空腹服用,以免延迟起效。从首次给药后12小时开始,每12小时给药50毫克Journavx,有或无食物;应该避免吃葡萄柚。建议肝功能损害患者和同时服用中度CYP3A抑制剂的患者调整剂量。
尚未对超过14天的中度至重度疼痛患者使用Journavx进行研究。治疗时间应根据患者个人目标尽可能缩短。
参考来源:
Vertex announces FDA approval of Journvax™ (suzetrigine), a first-in-class treatment for adults with moderate-to-severe acute pain. News release. Vertex. January 30, 2025.
注:以上资讯来源于网络,由香港济民药业整理编辑(如有错漏,请帮忙指正),只为提供全球最新上市药品的资讯,帮助中国患者了解国际新药动态,仅供医护人员内部讨论,不作任何用药依据,具体用药指引,请咨询主治医师。
如您发现本网站有文字编辑或内容错误,请点击此处发送(需要安装有foxmail或outlook支持),
或发邮件至:info@pidrug.com,香港济民药业感谢您的到访!
欢迎您添加香港济民药业微信,或在公众号内留言。