Tyenne(tocilizumab-aazg)是Actemra(tocilizumab,托珠单抗)的生物仿制药,除静脉(IV)给药方式外,目前还提供皮下(SC)给药方式。Tyenne是FDA批准的第一个具有静脉和皮下制剂的托珠单抗生物仿制药。
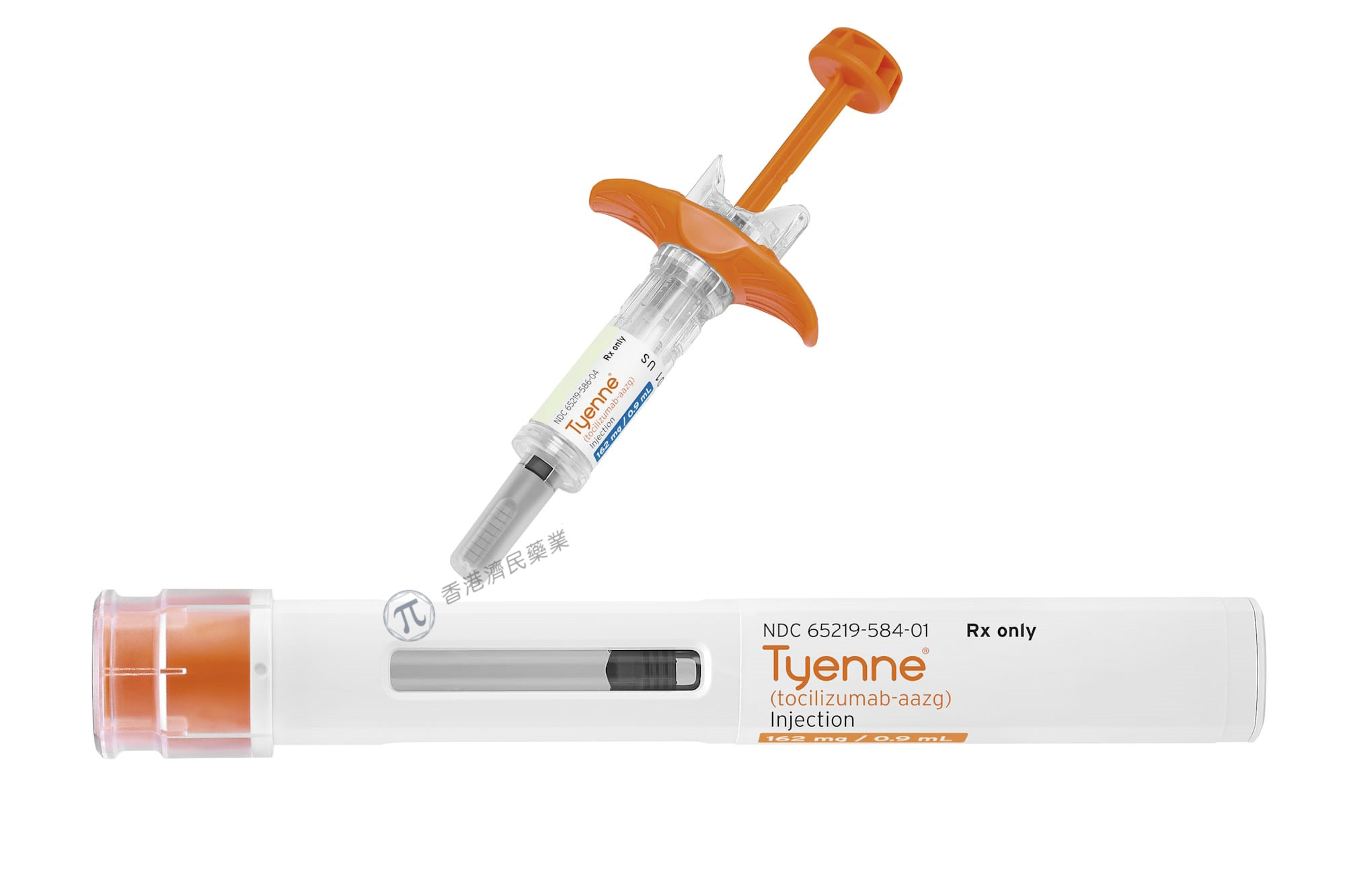 Tyenne的皮下制剂
Tyenne的皮下制剂
2024年3月,根据3期研究的数据(ClinicalTrials.gov标识符:NCT04512001),Tyenne获得了美国FDA的静脉和皮下给药批准。该试验在中度至重度活动性类风湿性关节炎患者中比较了tocilizumab-aazg和欧盟批准的托珠单抗。研究结果表明,这两种产品同样有效且安全。注意的是,已知对tocilizumab产品过敏的患者禁用本品。
Tyenne是一种白细胞介素-6(IL-6)受体拮抗剂,用于治疗以下疾病:
• 对一种或多种缓解疾病的抗风湿药物(DMARDs)反应不佳的中度至重度活动性类风湿性关节炎成年人;
• 成人巨细胞动脉炎;和
• 患有活动性多关节幼年特发性关节炎或活动性系统性幼年特发性关节炎的2岁及以上患者。
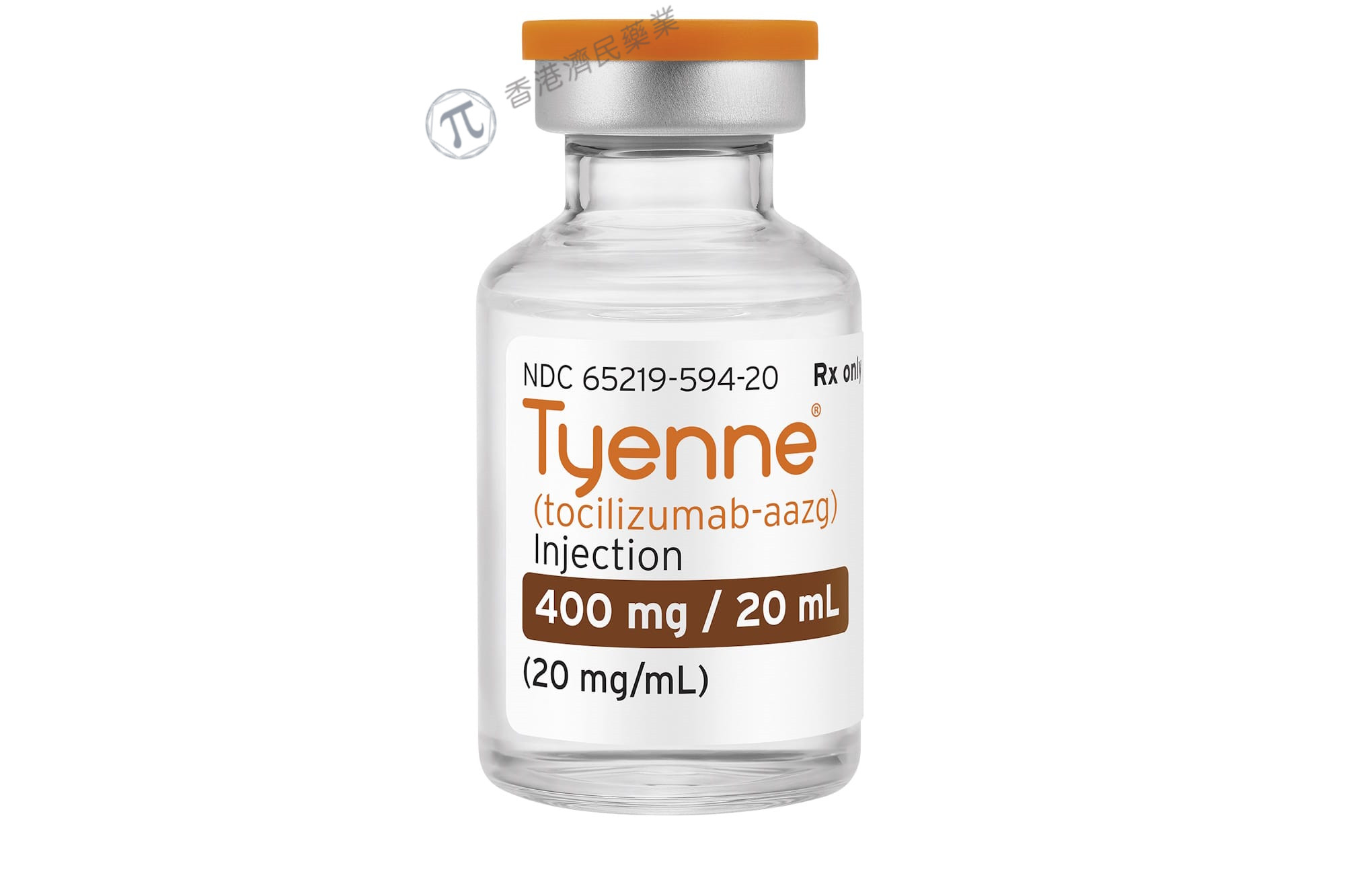 Tyenne的静脉制剂
Tyenne的静脉制剂
今年4月,Tyenne的静脉制剂已在美上市,以溶液(80毫克/4毫升、200毫克/10毫升和400毫克/20毫升)的形式提供在单剂量小瓶中,以便在静脉输注前进一步稀释。
现在Tyenne皮下制剂也已获FDA批准上市,可在自我给药预填充注射器和自动注射器中使用。皮下注射剂型有预充式注射器(162毫克/0.9毫升)和自动注射器(162毫克/0.9毫升)两种。患者在接受皮下注射技术方面的适当培训并经医疗保健提供者确认合适后,可以自行注射Tyenne。
参考来源:
Fresenius continues its Biopharma Momentum with launch of subcutaneous formulation of Tyenne® (tocilizumab-aazg) in the United States. News release. July 2, 2024.
注:以上资讯来源于网络,由香港济民药业整理编辑(如有错漏,请帮忙指正),只为提供全球最新上市药品的资讯,帮助中国患者了解国际新药动态,仅供医护人员内部讨论,不作任何用药依据,具体用药指引,请咨询主治医师。
如您发现本网站有文字编辑或内容错误,请点击此处发送(需要安装有foxmail或outlook支持),
或发邮件至:info@pidrug.com,香港济民药业感谢您的到访!
欢迎您添加香港济民药业微信,或在公众号内留言。




