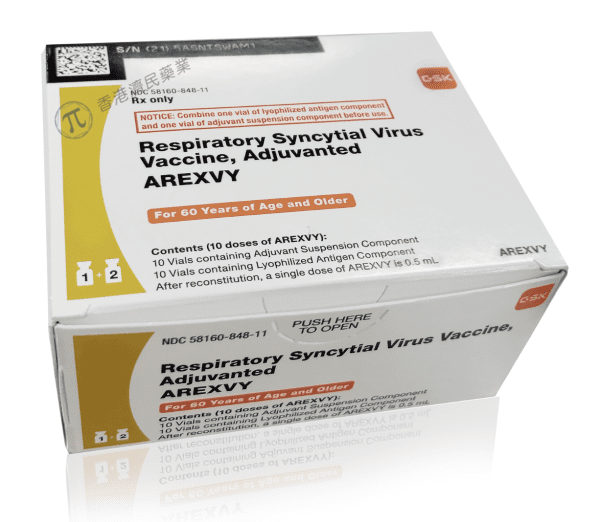
葛兰素史克(GSK plc)于6月7日宣布,美国FDA已批准Arexvy(含佐剂的呼吸道合胞病毒疫苗)用于预防50至59岁的呼吸道合胞病毒(RSV)下呼吸道疾病(LRTD),这些人患有RSV疾病的风险增加。此前,该疫苗仅适用于60岁及以上的成年人。
这是首款保护50-59岁高危人群的RSV疫苗。
扩大批准范围的依据是随机、观察者盲法、安慰剂对照的3期研究(ClinicalTrials.gov 标识符:NCT05590403)的数据,该研究包括约1520名年龄在50至59岁之间的个体。在研究参与者中,577人患有预先定义的稳定慢性疾病(例如慢性肺病、慢性心血管疾病、糖尿病、慢性肾病或慢性肝病)的RSV-LRTD风险较高。
研究结果表明,与60岁及以上成年人观察到的数据相比(主要终点),单剂量Arexvy在RSV风险较高的50岁及以上成年人中引发了非劣效免疫反应。
该研究还达到了其共同主要终点,表明50至59岁更广泛的成年人群体具有非劣效免疫反应。报告的最常见不良事件是疼痛、疲劳和头痛,这些不良事件是短暂的,强度较轻。
GSK首席科学官Tony Wood表示:“今天的批准反映了将RSV免疫的好处扩大到50至59岁高风险成年人的重要性。”“对于患有基础疾病的人来说,RSV可能会带来严重后果,因此我们很自豪能够成为第一个帮助他们预防RSV-LRTD的人。”
目前,Arexvy以两种成分提供:单剂量小瓶冻干抗原成分(粉末)和单剂量小瓶佐剂悬浮液成分(液体)(包装时不带注射器或针头)。疫苗复溶后通过肌肉注射给药。复溶后的单剂量为0.5毫升。
GSK还提交了监管申请,希望将其RSV疫苗的使用范围扩大到欧洲、日本和其他地区50-59岁高风险成年人,监管决定正在审查中。此外,评估Arexvy疫苗对18-49岁高风险成年人和18岁及以上免疫功能低下的成年人的免疫原性和安全性的试验预计将于2024年下半年公布。
参考来源:
US FDA approves expanded age indication for GSK’s Arexvy, the first respiratory syncytial virus (RSV) vaccine for adults aged 50-59 at increased risk. News release. GSK. June 7, 2024. Accessed June 10, 2024.
注:以上资讯来源于网络,由香港济民药业整理编辑(如有错漏,请帮忙指正),只为提供全球最新上市药品的资讯,帮助中国患者了解国际新药动态,仅供医护人员内部讨论,不作任何用药依据,具体用药指引,请咨询主治医师。
如您发现本网站有文字编辑或内容错误,请点击此处发送(需要安装有foxmail或outlook支持),
或发邮件至:info@pidrug.com,香港济民药业感谢您的到访!
欢迎您添加香港济民药业微信,或在公众号内留言。