全球人口中有2%至3%患有某种形式的银屑病,这是一种慢性炎症疾病,通常会影响皮肤、指甲和关节。高达90%的患者患有斑块型银屑病,其特征在于明显的圆形或椭圆形斑块,通常被银白色鳞片覆盖。
Enstilar是钙泊三醇(一种维生素D类似物)和二丙酸倍他米松(一种皮质类固醇)的复方产品,也是首款喷涂泡沫型银屑病药物,同时也是Daivobet软膏的“改进配方”,而Daivobet软膏是目前斑块型银屑病的标准治疗选择。
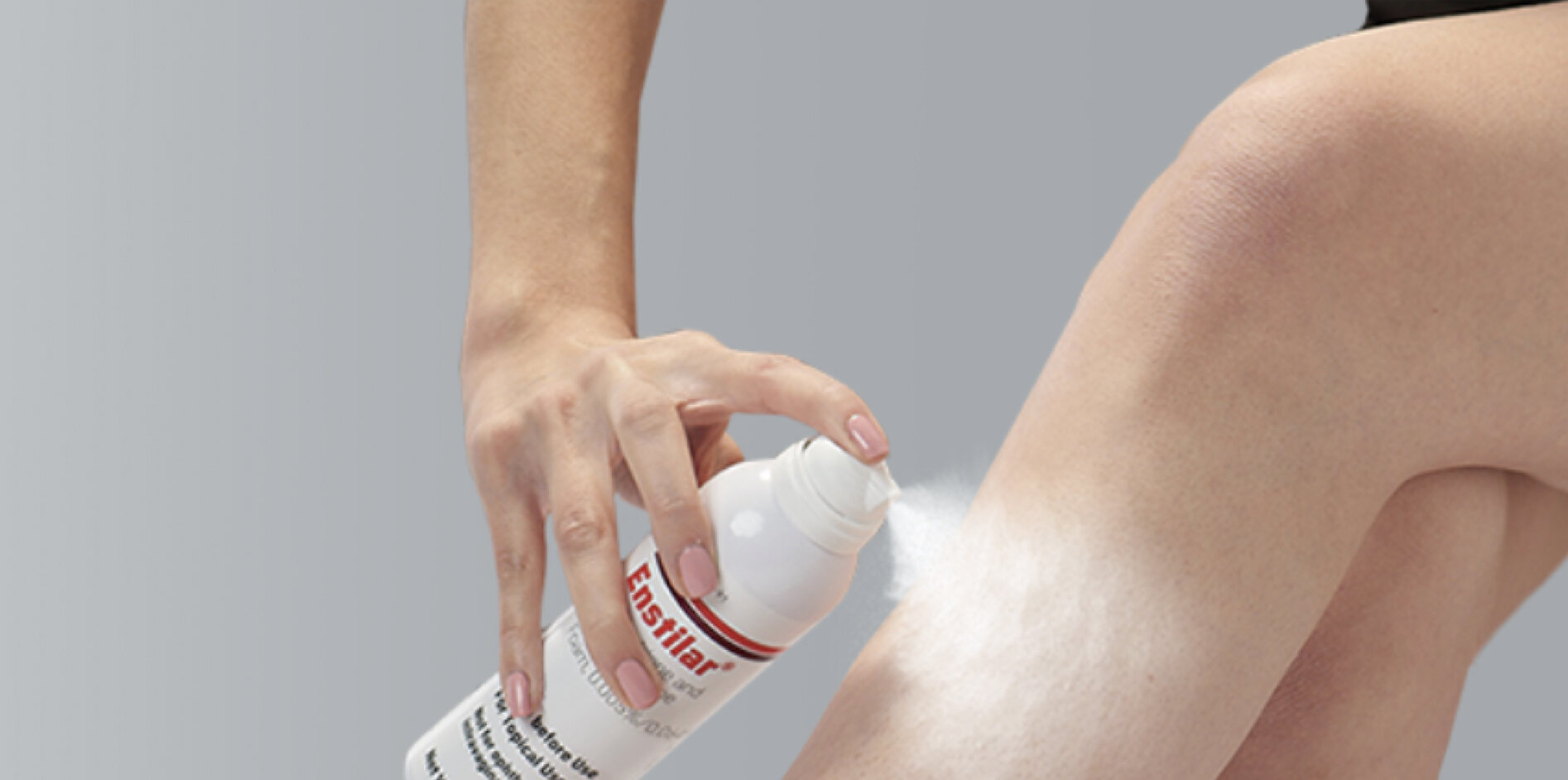
这是一种每天使用一次、不含酒精的泡沫状制剂,使用者可手握药罐喷在皮肤患处,方便携带与使用。
Enstilar首次于2015获得美国FDA批准,用于≥12岁患者斑块型银屑病的局部治疗。2020年10月26日,FDA批准Enstilar美国处方信息(USPI)更新,纳入PSO-LONG临床试验的数据,该试验评估了每周2次、长期使用(52周)Enstilar治疗成人斑块型银屑病。结果显示:与使用赋形剂泡沫的患者相比,长期使用Enstilar泡沫每周2次治疗的患者,其发生首次反应丧失时间较晚、 反应丧失的持续时间较短。在PSO-LONG试验中,Enstilar泡沫达到了主要终点:与赋形剂泡沫相比,推迟了发生首次反应丧失的时间(56天 VS 30天,p<0.001)。
在欧盟,Enstilar也已获得授权,可用于治疗成人寻常型银屑病长达四周,并作为对初始治疗有反应者的长期维持治疗。该疗法也在全球其他市场获得批准。
该试验是一项3期随机、研究者盲法、活性对照、平行组、多中心试验,比较了Enstilar和Daivobet软膏每天一次用于治疗患有稳定斑块型银屑病的成年中国受试者4周的疗效和安全性。这项试验在中国的39个研究点共招募了604名患者。
研究的主要目的是评估Enstilar与Daivobet软膏在稳定斑块型银屑病的严重程度和范围方面的疗效。次要目标评估治疗安全性。探索性目标包括评估健康相关的生活质量。
结果显示,Enstilar在主要终点方面优于Daivobet,证明在降低稳定斑块型银屑病的严重程度和范围方面具有改善的功效。
此外,这两种治疗方法均具有良好的耐受性,并且其安全性与之前的试验结果一致。
试验结果将支持利奥制药向中国药品监管局提交Enstilar的上市申请。
此次试验的详细结果将在晚些时候提交用于科学展示和出版。
参考来源:
ClinicalTrials.gov: A Study to Investigate Efficacy and Safety With LEO 90100 Compared With Daivobet® Ointment in Adult Chinese Subjects With Stable Plaque Psoriasis | ClinicalTrials.gov (Accessed May 2024)
注:以上资讯来源于网络,由香港济民药业整理编辑(如有错漏,请帮忙指正),只为提供全球最新上市药品的资讯,帮助中国患者了解国际新药动态,仅供医护人员内部讨论,不作任何用药依据,具体用药指引,请咨询主治医师。
如您发现本网站有文字编辑或内容错误,请点击此处发送(需要安装有foxmail或outlook支持),
或发邮件至:info@pidrug.com,香港济民药业感谢您的到访!
欢迎您添加香港济民药业微信,或在公众号内留言。